胃肠间质瘤是一种较为常见的恶性胃肠道肿瘤,目前胃肠间质瘤的治疗主要通过手术加药物的疗法。手术能够切除大部分的胃肠间质瘤的实体瘤,但手术很难完全切除病灶,这直接导致胃肠间质瘤的术后高复发率。因此,术后配合药物的治疗才能取得较好的治疗效果,目前医学界鼓励采用靶向药物用于术后的巩固治疗。病理学研究证明激酶C-KIT是胃肠间质瘤治疗的有效靶点,针对此激酶,目前已有两例靶向药物批准用于胃肠间质瘤的治疗,他们分别是格列卫(Imatinib)和索坦(Sunitinib)。由于这两个药物均是激酶多靶点抑制剂,关于其脱靶现象所引起的毒副作用也一直备受关注:Imatinib由于抑制激酶C-KIT的同时也会很强地抑制激酶BCR-abl的活性,这会引起很大的潜在心脏毒性;Sunitinib也存在一个问题就是能够同时抑制C-KIT和FLT3,这会较为强烈的引起骨髓抑制毒性。因此,基于高选择性的C-KIT激酶抑制剂的胃肠间质瘤药物是此类创新药物开发的较为理想的选择。
鉴于此,中国科学院合肥物质科学研究院强磁场中心刘青松研究员课题组与刘静研究员课题组合作,开发出新一代针对胃肠间质瘤的高选择性激酶C-KIT抑制剂CHMFL-KIT-110, CHMFL-KIT-110能够强烈抑制激酶C-KIT的磷酸化(IC50=99nM),同时对BCR-abl特征细胞系K562和FLT3 特征细胞系TEL-FLT3 BaF3均不显示抑制作用。在人类468种激酶的选择性测试中, CHMFL-KIT-110显示出较小的脱靶作用(S score(1)=0.01),说明其具有很高的选择性。药代动力学研究显示CHMFL-KIT-110具有良好的药代动力学参数,大鼠口服半衰期为4.11小时,口服绝对生物利用度为36%。在小鼠胃肠间质瘤肿瘤模型实验中,CHMFL-KIT-110展示出明显的对胃肠间质瘤的生长抑制作用(100mg/kg/day, 21day:TGI=49%)。研究成果发表在美国化学会药物化学核心期刊Journal of Medicinal Chemistry上(DOI: 10.1021/acs.jmedchem.6b00200)。
该研究成果已经申请中国发明专利(专利号:201610210424.X),并且正在与安徽合源药业联合进行国家1类创新药物开发。该项目由助理研究员王强、博士生刘飞扬、研究实习员王蓓蕾、助理研究员邹凤鸣以及研究实习员陈程等协作完成。
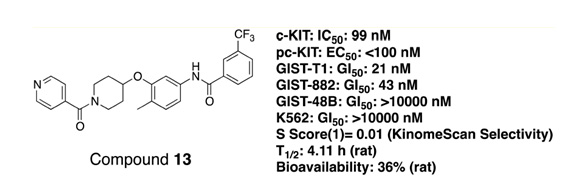
CHMFL-KIT-110(Compound 13)化学结构以及其生物活性数据
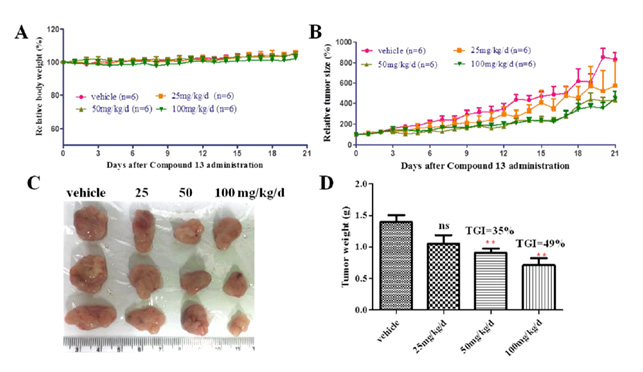
CHMFL-KIT-110对胃肠间质瘤小鼠肿瘤模型的作用效果
