细胞周期蛋白依赖性激酶9(CDK9)作为p-TEFb的亚单位参与转录的延长过程,在转录过程中发挥重要作用。CDK9激酶调控短寿命抗凋亡蛋白的RNA转录,因此它在多种癌症中是重要的作用靶点。由于CDK激酶家族成员众多,有超过20种亚型之间的序列存在高度保守性和空间结构相似性,导致目前许多CDK9抑制剂的选择性不高,从而引起脱靶毒副作用。因此发展高选择性和高活性的CDK9抑制剂对于基础研究以及临床应用都具有重要意义。
在本项工作中,研究人员通过对CDK9激酶结构进行分析,采用以结构为基础的药物设计理念发展了一种高选择性、高活性的CDK9激酶抑制剂JSH-150。实验结果显示JSH-150在CDK家族成员中取得很好的选择性,JSH-150对CDK9的活性是对CDK家族其它成员的300-10000倍,其能够有效抑制CDK9激酶的活性(IC50 = 1 nM)。
此外与其它468种激酶的结合强度测试结果显示,JSH-150在激酶组中也具有极高的选择性。JSH-150在不同的癌症细胞系如黑色素瘤、鳞癌、胃肠间质瘤、结直肠癌、B细胞淋巴瘤、急性髓性白血病以及慢性淋巴性白血病细胞系中都表现出很强的抗增殖作用,初步展现了其广谱抗肿瘤活性的潜力。此外,在急性髓性白血病细胞MV4-11的小鼠皮下移植瘤模型上对药物的体内抗肿瘤活性进行检测,在用药20mg/kg的剂量下JSH-150对肿瘤表现出很好的抑制效果。
该研究工作主要由博士后吴云、博士研究生王蓓蕾、吴佳昕以及陈程、助理研究员邹凤鸣等人共同完成。该研究获得了国家自然科学基金、万人计划青年拔尖人才项目、中科院前沿科学重点研究项目、中国博士后基金和安徽省自然科学基金等项目的支持。
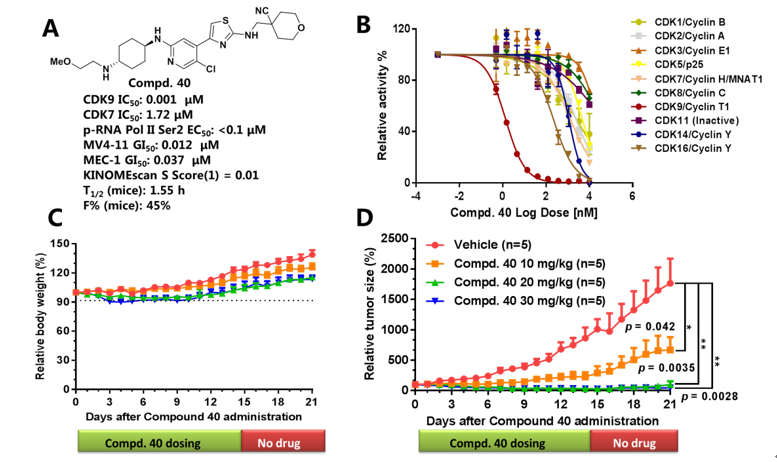
JSH-150(compd. 40)的生物学表征及对MV4-11肿瘤细胞小鼠模型的抑瘤作用
