近日,强磁场中心张钠研究员课题组首次运用核磁共振(NMR)技术解析由端粒DNA序列d(G2T4G4T4G4)与短链d(TG4A)探针形成的分子间V-形G-四链体复合物结构,发现新型短链DNA探针能够特异性识别包含V-shape关键碱基序列的端粒DNA,具有潜在抗癌前景。该研究成果在线发表于国际期刊Nucleic Acids Research(doi:10.1093/nar/gky1167)。
端粒DNA形成G-四链体结构与抑制癌症密切相关,是优良抗癌靶点。G-四链体中除了经典的连接环区域外,还存在独特的V-形支架结构域,其不包含任何中间残基,却可以跨越三个G-四分体平面。这种V-形支架可以使两个相邻碱基之间糖磷骨架链的方向发生急剧逆转,同时又参与形成G-四分体核心的氢键连接。这些特性使得这种V-形支架本身与众不同,因此本质上作为药物设计靶标时更容易被特异性识别。端粒DNA由重复碱基序列单元构成,这就造成其被传统反义互补链探针识别时,通常选择性不理想。对此,张钠课题组预测作为传统反义互补链的替代方法,由两个不同的DNA寡聚体能够形成分子间的G-四链体,其中较长的DNA寡聚体作为靶标被短的富含G的DNA探针片段捕获,进而有助于更特异性识别端粒DNA中富含连续G序列的重复结构基序。然而,此前这种由不同长度的DNA寡聚体组成的分子间V-形G-四链体结构尚未有报道。
在本项工作中,研究人员首先对尖毛虫的端粒序列d(G2T4G4T4G4)和探针d(TGGGGA)形成的复合物进行了液体核磁共振结构解析,证明该复合物是一种新型非对称分子间V-形G-四链体。通过核磁共振的竞争结合实验,发现采用该构型与常规的G-四链体构型相比热力学更加稳定且动力学形成速度快。后续研究人员进一步通过对原始序列进行碱基突变处理,证明在人源端粒DNA的天然突变体中,只要具备d(G2NG3NG4)特征的序列,明显比其他序列更容易被探针识别和捕获,从而为抗癌靶标端粒DNA区域的靶向探针设计提供了一种新的思路和理论支持。
该研究工作由论文第一作者博士后万婵娟,以及博士研究生付文强、景海涛,通讯作者张钠研究员等人共同完成。该研究获得了国家自然科学基金青年科学基金,国家自然科学基金联合基金,国家重点研发计划项目等多个项目的支持。核磁共振部分工作在稳态强磁场实验装置上开展实施。
文章链接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gky1167/5184730。
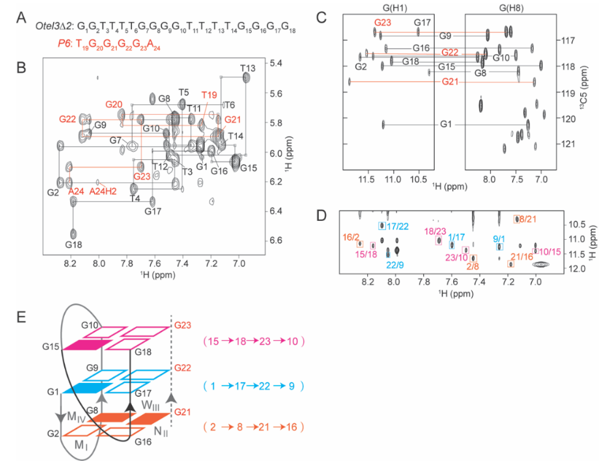
d(G2T4G4T4G4)与 d(TG4A)形成V-形G-四链体复合物的相关NMR实验
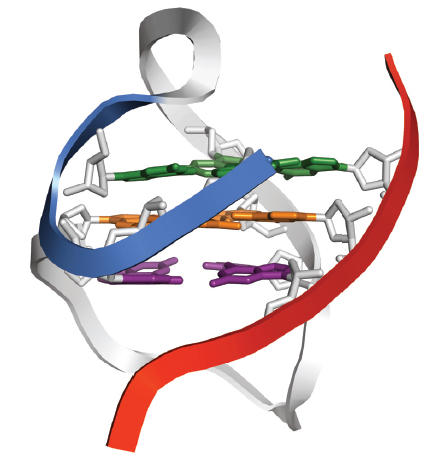
V-形G-四链体DNA复合物结构三维模型(PDB: 6A7Y)
