近期,中科院合肥研究院医学物理与技术中心辐射生物医学研究室韩伟团队在低温等离子体肿瘤治疗方面再次取得重要突破,首次报导大气压低温等离子体可有效诱导肿瘤细胞发生焦亡(Pyroptosis)。相关论文“Cold Atmospheric Plasma Induces GSDME-Dependent Pyroptotic Signaling Pathway via ROS Generation in Tumor Cells”发表于Cell Death & Disease上。该期刊系Nature出版集团旗下的医学生命科学期刊之一,主要关注细胞死亡和转化医学研究等领域的原创性研究。
等离子体医学近年来蓬勃发展,等离子体肿瘤治疗被视为一种新兴的肿瘤治疗方式。以往大量研究表明,等离子体通过诱导肿瘤细胞发生典型凋亡或坏死等形式的细胞死亡,达到抑制肿瘤生长及“清除”肿瘤的效果。细胞焦亡是一种炎性细胞程序性死亡,以往细胞焦亡研究多集中于机体固有免疫。2017年,邵峰院士首次发现化疗药物可导致肿瘤细胞发生GSDME介导的焦亡,不同于凋亡,肿瘤细胞的焦亡发生更为快速,容易激活体内免疫系统。
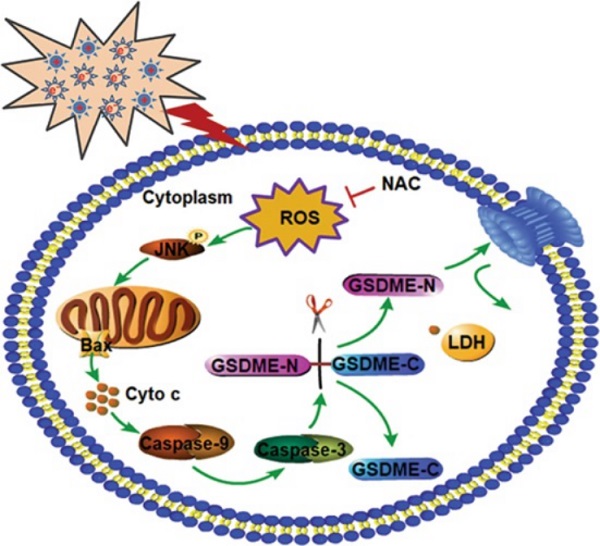
该研究通过筛查三个瘤种共计十五株肿瘤细胞系,发现等离子体对肿瘤细胞的杀伤效果与细胞内GSDME的表达水平呈正相关;相关分子机制研究表明,等离子体通过激活ROS/JNK/Cytochrome C/Caspse-9/Caspse-3信号通路,进一步切割GSDME,导致肿瘤细胞发生焦亡型细胞死亡。
该研究不仅首次报导了等离子体致死肿瘤细胞的新型死亡方式——焦亡,也是首次报导物理治疗方法可导致肿瘤细胞发生焦亡。研究结果进一步增加了对等离子体肿瘤治疗机制的深入了解,为凋亡抵抗型肿瘤提供了一种新的治疗策略。
该研究工作由辐射生物医学研究室杨小枘和陈国栋共同完成。研究得到国家重点研发计划、安徽省自然科学基金资助。
文章链接:https://www.nature.com/articles/s41419-020-2459-3