近日,中科院合肥研究院健康所刘青松药学团队研发出一种针对B细胞淋巴瘤的高活性、高选择性EZH2抑制剂IHMT-EZH2-115。该研究成果在线发表于药物化学国际知名期刊Journal of Medicinal Chemistry。
弥漫性大B细胞淋巴瘤(DLBCL)是成人淋巴瘤中最常见的一种亚型,在中国占所有淋巴瘤的40%左右。 EZH2是一种组蛋白赖氨酸甲基转移酶,研究表明7%的滤泡性淋巴瘤和20%左右的DLBCL中检测到EZH2上位于具有催化活性的SET结构域内的641位酪氨酸(Y641)编码基因功能获得性突变,增强其二甲基化和三甲基化的能力,从而抑制基因转录,沉默细胞周期抑制蛋白和B淋巴细胞分化相关基因,导致生发中心B淋巴细胞增殖和分化异常,因而在DLBCL和滤泡性淋巴瘤的发生中起重要作用。此外,EZH2过度表达也与前列腺癌、乳腺癌、肾癌、肺癌、多发性骨髓瘤等多种癌症相关。目前唯一上市的EZH2抑制剂EPZ6438(Tazemetostat)在2020年6月被FDA批准用于滤泡性淋巴瘤的治疗,但目前国内外尚未有靶向EZH2的小分子抑制剂被批准用于DLBCL的治疗,因此开发新型的EZH2 抑制剂仍然具有强烈的临床需求。
在本项研究工作中,科研团队结合计算机辅助药物设计方法,利用药物化学的设计合成策略,对EPZ6438结构中与EZH2蛋白配体结合口袋相结合的片段,以及伸向蛋白与溶剂域相互作用的片段进行了构效关系研究,并通过一系列体外生物活性检测,发现了先导化合物IHMT-EZH2-115。蛋白及细胞层次的研究表明,IHMT-EZH2-115能有效抑制野生型EZH2以及临床上多种常见的EZH2突变体,包括EZH2 A677G、EZH2 Y641F、EZH2 Y641N和EZH2 Y641S,并且该抑制剂在组蛋白甲基转移酶中显示出很好的选择性。此外,该化合物对hERG钾离子通道没有明显的抑制作用,初步说明其不会导致潜在的心脏毒性。
体内药代动力学研究表明,IHMT-EZH2-115适合进行口服给药。体内药效研究结果显示,在两种EZH2突变体的DLBCL细胞Pfeiffer(EZH2 A677G)和Karpas-422(EZH2 Y641N)构建的小鼠皮下移植瘤模型中,IHMT-EZH2-115均能剂量依赖性地有效抑制肿瘤生长,在200 mg/kg每天两次的口服剂量下,抑瘤率(TGI)分别达到100%和97.3%。该研究成果已经申请了发明专利,目前已完成了临床前研究并进行了产业转化。
该研究工作获得了国家自然科学基金、安徽省杰出青年科学基金、中科院青促会、中科院前沿科学重点研究计划等项目的支持。
文章链接 :https://pubs.acs.org/doi/10.1021/acs.jmedchem.1c01154
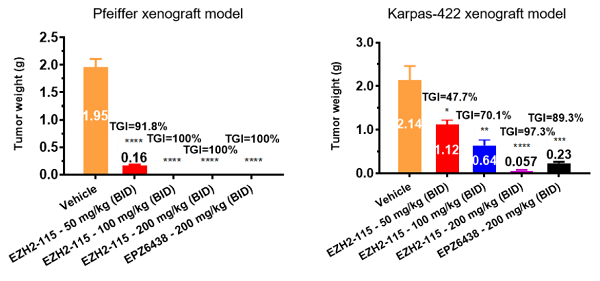
IHMT-EZH2-115在小鼠肿瘤模型上的药效研究
