近日,中科院合肥研究院强磁场中心王俊峰研究员课题组,在研究自然界趋磁细菌生物矿化机制的基础上,仿生合成具有高效磁靶向及肿瘤组织穿透性的软铁磁类磁小体纳米材料,相关成果发表在美国科学院院刊(Proceedings of the National Academy of Sciences of the United States of America,PNAS)上。
抗肿瘤药物的靶向递送可以有效提高药物的疗效,降低药物的毒性,是现代生物医学发展的一个重要研究方向。由于复杂肿瘤组织环境产生的隙流体压力增加以及组织中的致密细胞外基质的限制,目前的纳米药物平均肿瘤靶向效率均低于1%,构成了肿瘤治疗中的瓶颈之一。近年来,随着磁性纳米药物的发展,利用施加外部磁场提高磁性纳米药物靶向效率,即磁靶向,成为一种重要且安全的物理干预策略。
地球上许多动物能利用地磁场导航,如鸽子、海龟、蜥蜴等都发展出独特的磁导航机制长途迁徙。同样,原核生物中的趋磁细菌(Magnetotactic bacteria)也能够响应地磁场定向游弋。趋磁细菌具有鞭毛和独特的细胞内结构—磁小体(magnetosome):由膜包被的纳米尺寸的磁铁矿颗粒构成的磁小体链状排布,作为细菌的“生物罗盘”。结合鞭毛的动力系统,趋磁细菌可以在地磁场或人工磁场中沿磁场方向定向移动。趋磁细菌从周围环境中获取铁元素,在严格的生物矿化机制调控下合成四氧化三铁纳米颗粒,并组装成功能化的磁小体,可以快速地响应外部磁场。磁小体粒径分布约在40-50nm,具有高度均一性。相比目前工业生产的磁性纳米材料,磁小体在磁性能、生物兼容性、稳定性和磁热效等指标具有明显优势。因此,磁小体作为磁靶向的磁性纳米颗粒,具有广泛的应用前景。然而,天然磁小体颗粒之间的强磁相互作用导致从趋磁细菌中直接分离提取的磁小体在体外环境中十分容易聚集沉淀,从而阻碍了它们穿透病变组织的能力,并且在血管中的沉积也存在潜在的危险和生物毒性。因此,合成尺寸小但保留了天然磁小体软铁磁特点的类磁小体纳米材料,不仅是对仿生合成技术的挑战,在生物医学应用上也有着巨大价值。
前期研究表明,趋磁细菌基因编码的一个特殊蛋白Mms6,在调控磁小体晶体形貌中起到至关重要的作用。成熟的Mms6蛋白在N端有一个疏水区域,预测为膜结合区;C端有一个高酸性的结构域,推测是其与铁离子结合的区域,参与磁小体晶体的形成。
在本研究工作中,基于课题组前期对磁小体生物矿化机制的系统性研究(Journal of Materials Chemistry B, 2017, 5(16): 2888-2895. ; ACS Applied Materials & Interfaces, 2020, 12(51): 56701-56711.),研究人员提出了类磁小体仿生合成的新策略:考虑到趋磁细菌生物矿化所需的两个关键因素:磁小体膜与磁小体调控蛋白,研究人员通过在反相胶束体系中引入Mms6蛋白,构建了一个类似天然磁小体囊泡的纳米反应器,在体外重构了趋磁细菌磁小体生物矿化的微环境。通过这一方法,仿生矿化合成的类磁小体晶体成具有与天然磁小体一致的立方八面体的晶型以及类似的磁学性质及高饱和磁化强度,可以快速响应外部磁场,同时,仿生合成的类磁小体还具有优异的单分散性、均一的小尺寸和良好的亲水溶性。体内MRI实验与组织分布实验结果表明,与其他磁性纳米药物相比,仿生合成的类磁小体在肿瘤组织中的靶向性与穿透性提高了一个数量级。综上所述,这项工作不仅为纳米药物磁靶向递送提供一个高效的载体,也为体外研究趋磁细菌生物矿化机制提供了新的模式系统。
强磁场中心助理研究员马坤、博士后许帅、博士生陶童祥,合肥研究院健康所副研究员钱俊超为文章的共同第一作者。强磁场中心王俊峰研究员为文章的通讯作者。强磁场中心张欣研究员、谢灿研究员以及健康所王宏志研究员共同参与此项课题研究。该项研究获得国家自然科学基金、科技部重大专项、中科院合肥研究院院长基金以及国家重大科技基础设施“稳态强磁场实验装置”(SHMFF)的支持。
文章链接:www.pnas.org/doi/10.1073/pnas.2211228119
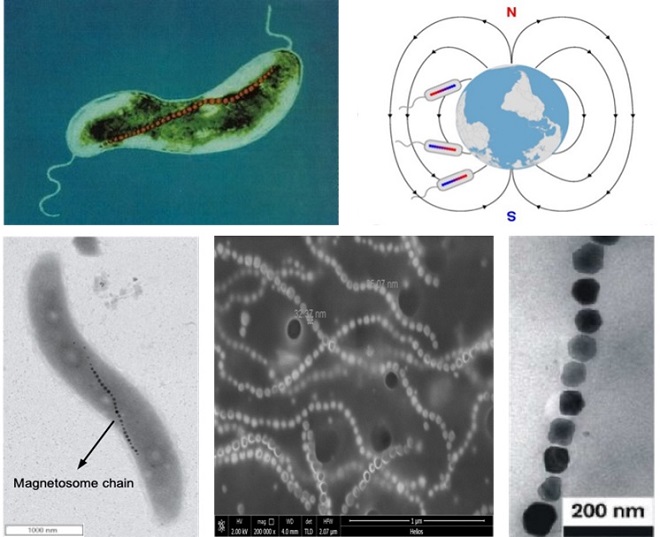
图1 :趋磁细菌磁导航及其链状排布的磁小体“生物罗盘”
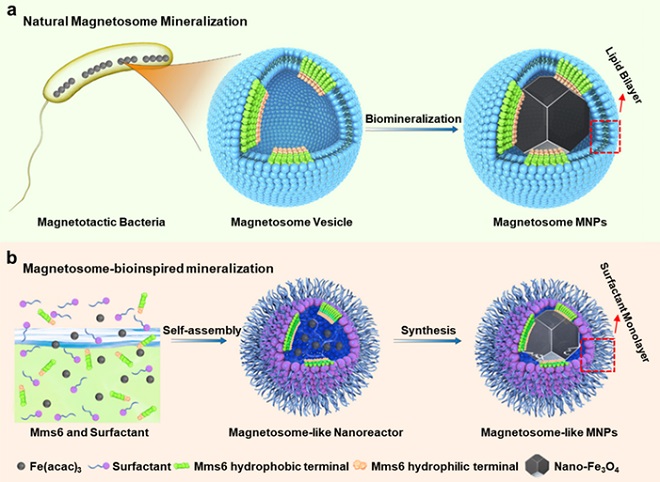
图2:模拟趋磁细菌生物矿化过程基于生物矿化调控蛋白Mms6 构建的反向微囊纳米反应器
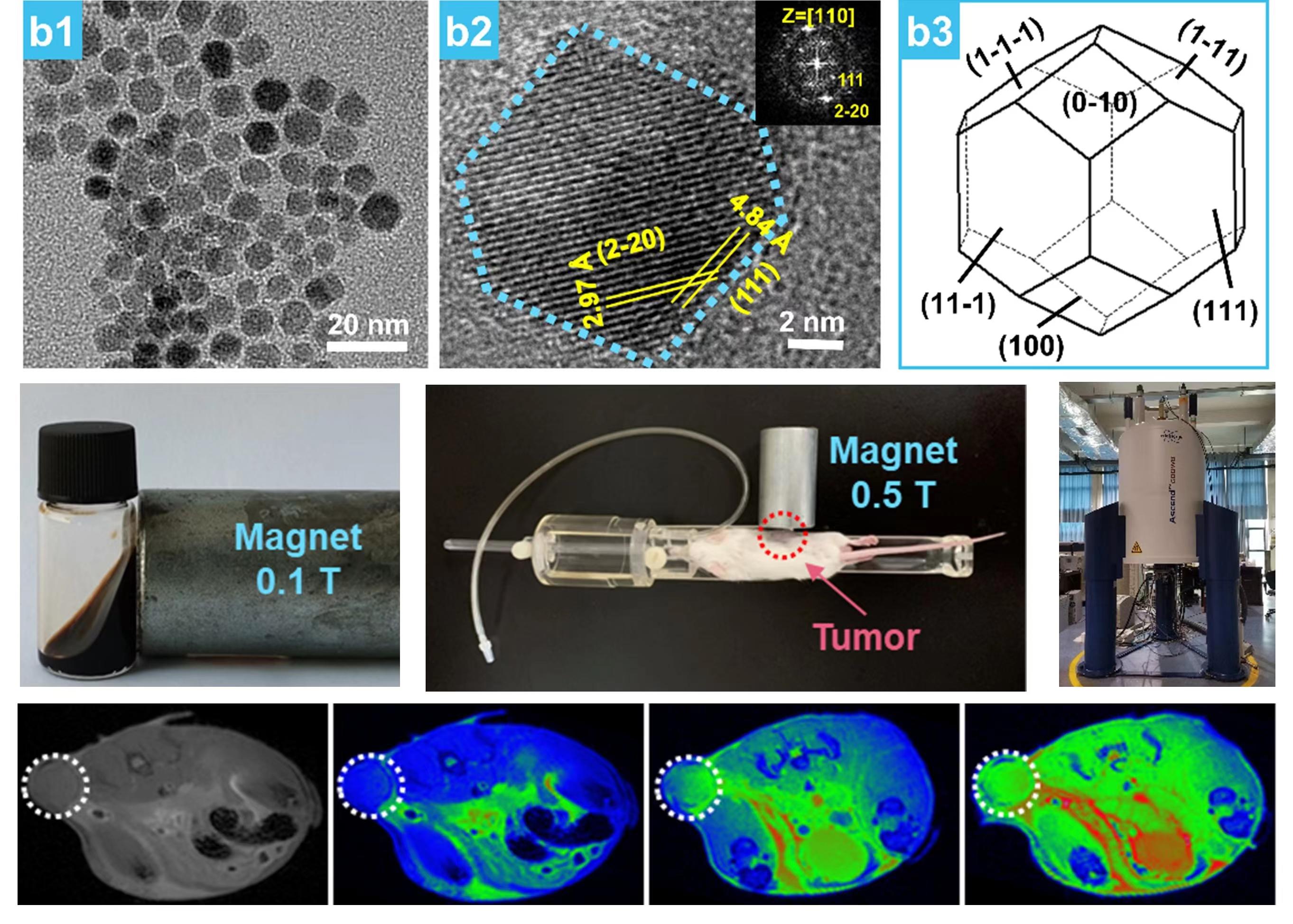
图3:类磁小体具有与天然磁小体一样晶体形貌与磁学特性,可以高效响应外加磁场,实现针对肿瘤组织的靶向富集与高效渗透。(MRI实验在稳态强磁场实验装置SM3上完成)
