近日,强磁场科学中心刘静研究员课题组和刘青松研究员课题组针对慢性髓细胞白血病和胃肠间质瘤研发出一种新型的具有独特结合模式的高活性BCR-ABL/c-KIT激酶双靶点抑制剂CHMFL-ABL/KIT-155。该研究成果以Discovery of 4-Methyl-N-(4-((4-methylpiperazin-1-yl)methyl)-3-(trifluoromethyl) phenyl)-3-((1-nicotinoylpiperidin-4-yl)oxy)benzamide(CHMFL-ABL/KIT-155) as a Novel Highly Potent Type II ABL/KIT Dual Kinase Inhibitor with a Distinct Hinge Binding为题在线发表于美国化学会药物化学核心期刊Journal of Medicinal Chemistry(DOI: 10.1021/acs.jmedchem.6b01290)。
慢性髓细胞白血病(CML)是骨髓造血干细胞克隆性增殖形成的恶性癌症,约占成人白血病的15%。研究表明BCR-ABL融合基因的异常表达及突变在CML的发生、发展及预后过程中起到关键作用,而BCR-ABL激酶是经过临床验证的治疗CML的有效药物作用靶点。胃肠间质瘤是一种恶性程度极高的胃肠道癌症,病理学研究表明c-KIT激酶的过度表达及异常激活在胃肠间质瘤的发生、发展以及恶化中起到主导性的作用。目前,靶向BCR-ABL/c-KIT激酶的慢性髓细胞白血病和胃肠间质瘤的小分子抑制剂药物如伊马替尼已经在临床上大量使用并取得了良好的治疗效果,但同时也存在着进口药物价格昂贵和产生耐药等局限性。因此,临床上仍然需要具有我国自主知识产权的“Me Too”或者“Me Better”药物用于相关疾病的治疗。
该团队继前期研发的高选择性BCR-ABL激酶抑制剂CHMFL-ABL-053/CHMFL-ABL-074和高选择性c-KIT激酶抑制剂CHMFL-KIT-110之后,通过基于结构药物设计等方法又成功发现了一种新型高活性的靶向BCR-ABL/c-KIT的II型激酶抑制剂CHMFL-ABL/KIT-155。该抑制剂在体外对于BCR-ABL/c-KIT激酶展现出极强的抑制活性(IC50: 46 nM/75 nM),并可以有效抑制BCR-ABL阳性白血病细胞以及胃肠间质瘤细胞的增殖。药代动力学研究表明其口服半衰期为2.8h,绝对生物利用度为47%, 具有较好的成药性。在临床前动物模型实验中,CHMFL-ABL/KIT-155可以有效抑制慢性髓细胞白血病肿瘤和胃肠间质瘤在小鼠体内的增长,100mg/kg/d的剂量针对以上两种肿瘤的抑制率分别为66.8%(优于伊马替尼的31.9%抑瘤率)和46.5%,同时对小鼠并未表现出明显的毒性。
目前,该研究成果已经申请了专利保护。
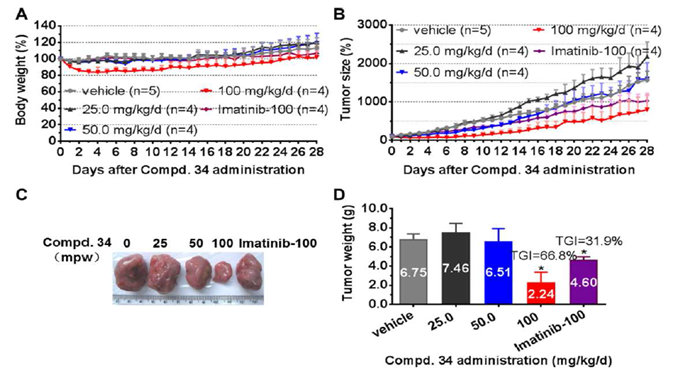
CHMFL-ABL/KIT-155(化合物34)对于慢性髓细胞白血病的小鼠肿瘤模型的作用效果
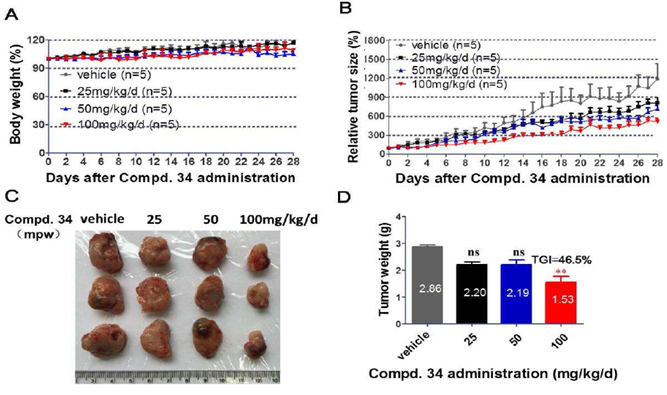
CHMFL-ABL/KIT-155(化合物34)对于胃肠间质瘤的小鼠肿瘤模型的作用效果
