近日,中国科学院合肥物质院健康所/合肥肿瘤医院王宏志研究员、洪波研究员与安徽医科大学第一附属医院陈江明副主任医师合作,发现前列腺素E合酶3(PTGES3)在肝细胞癌中发挥非经典核内转录调控功能,通过PTGES3/SP1/TGF-β信号轴,同时驱动肿瘤增殖与免疫抑制性微环境重塑。相关研究成果以“Nuclear prostaglandin E synthase 3 promotes hepatocellular carcinoma growth with immunosuppressive macrophage polarization via the SP1/TGF-β axis”为题,发表于Molecular Biomedicine。
PTGES3(又称p23)传统上被认为是细胞质中HSP90分子伴侣的辅助因子。尽管近年来研究发现其可转位至细胞核,但其在肿瘤中作为核内转录调控因子的角色此前鲜有报道。肝细胞癌的临床治疗面临肿瘤增殖与免疫抑制微环境协同建立的双重挑战,然而驱动这一过程的核内上游分子机制长期不明。
研究团队通过多个公共数据集和临床标本验证,确认PTGES3在肝癌中显著高表达并与患者不良预后独立相关。功能实验表明,PTGES3通过PI3K/AKT/mTOR通路促进肝癌细胞增殖与迁移。在DEN诱导的肝癌模型中,通过感染肝细胞特异性AAV-TBG-shPtges3病毒,研究发现Ptges3敲低显著抑制肿瘤生长,单细胞RNA测序揭示其表达下调可重塑肿瘤免疫微环境,表现为巨噬细胞M2型极化受抑。机制上,研究团队整合CUT&Tag、EMSA、ChIP-qPCR和双荧光素酶报告基因等技术,发现PTGES3在核内直接结合SP1启动子G-rich基序驱动SP1转录,SP1进一步上调TGF-β分泌,一方面通过自分泌激活PI3K/AKT/mTOR通路维持肿瘤增殖,另一方面以旁分泌方式诱导巨噬细胞M2极化。值得注意的是,HSP90抑制剂无法逆转该效应,而TGF-β受体抑制剂可有效阻断,证实该功能独立于PTGES3的经典分子伴侣活性。
综上所述,该研究揭示了PTGES3作为核内转录调控因子驱动肝细胞癌增殖与免疫抑制的新功能,阐明了其通过SP1/TGF-β信号轴耦联肿瘤增殖与免疫逃逸的新机制,为肝癌靶向治疗与免疫治疗的联合策略提供了潜在干预靶点。
博士研究生王年飞为论文第一作者,王宏志研究员、洪波研究员和陈江明副主任医师为论文通讯作者。该研究得到了中国科学院合肥肿瘤医院单病种科研攻关项目的资助。
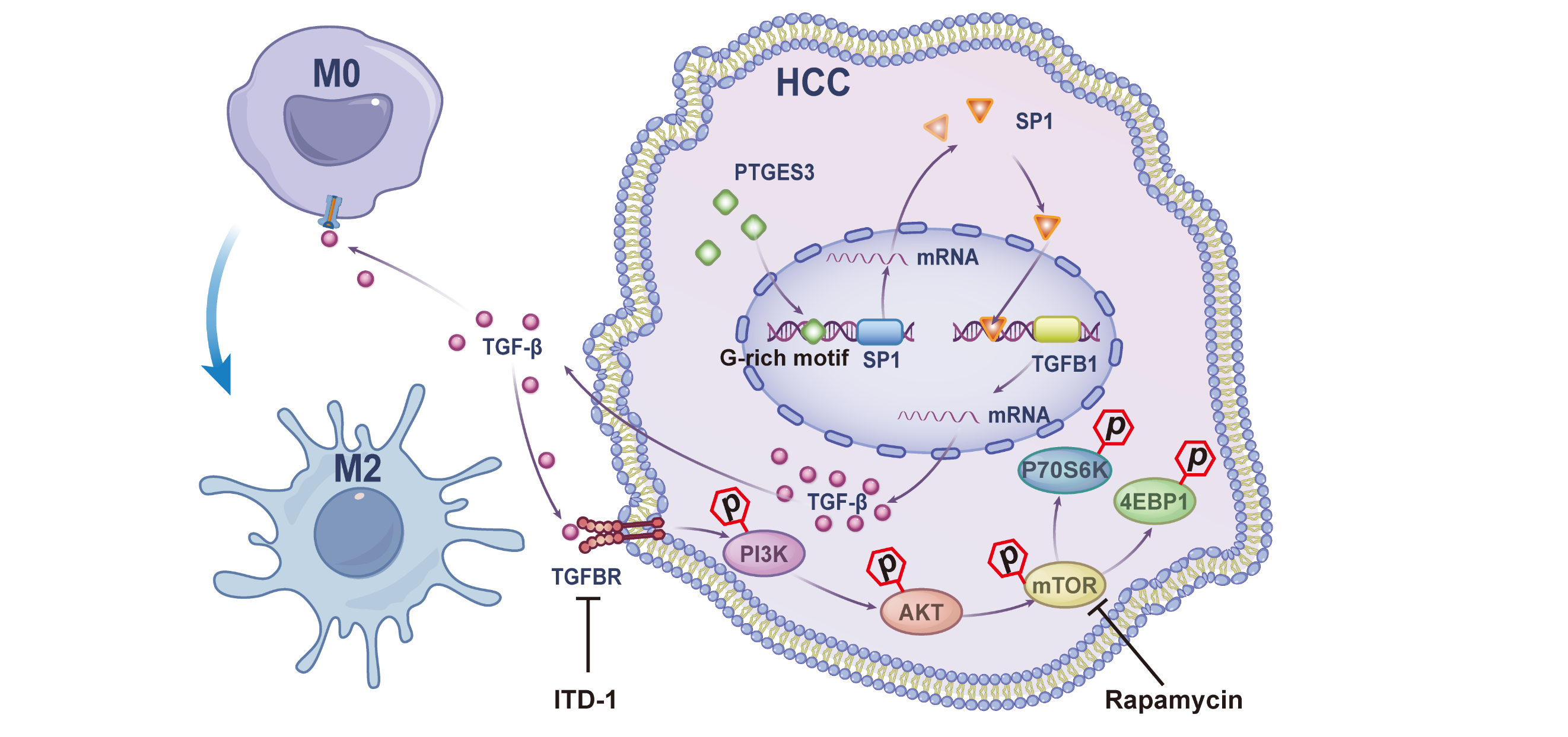
图. 示意图显示PTGES3核内转录调控促进肝细胞癌增殖与免疫抑制的新机制
