
近日,中科院合肥研究院健康与医学技术研究所刘青松研究员、刘静研究员药学团队开发出了针对B细胞性非霍奇金淋巴瘤的新一代高选择性、高活性BTK激酶抑制剂CHMFL-BTK-85。这是继CHMFL-BTK-01和CHMFL-BTK-11之后,该团队在BTK激酶抑制剂研究中取得的又一进展。该成果目前在线发表于国际期刊Signal Transduction and Targeted Therapy。
B细胞性非霍奇金淋巴瘤是一种常见的恶性癌症,发病率为10-15/10万,其发病率随年龄增加,且病人生存率较低。布鲁顿酪氨酸激酶(Bruton's tyrosine kinase,BTK)是一种非受体酪氨酸激酶,大量研究表明BTK激酶的过度表达和活化是引起这类癌症的主要致病因素之一。尽管首个获批上市的BTK激酶抑制剂依鲁替尼(ibrutinib)在靶向治疗B细胞性非霍奇金淋巴瘤上取得了重大突破,但依鲁替尼除了抑制BTK激酶以外,还会抑制EGFR、ITK、JAK3、HER2等其他重要信号通路的蛋白,从而引发一些副作用的出现,如对ITK的抑制会限制免疫细胞介导的ADCC(antibody-dependent cell-mediated cytotoxicity,抗体依赖性的细胞介导的细胞毒作用)效应。因此,开发高选择性的BTK激酶抑制剂具有重要的临床价值。
在前期研究中,研究团队已通过药物设计及高通量筛选的方法开发了一系列具有自主知识产权的BTK激酶抑制剂,包括CHMFL-BTK-01和CHMFL-BTK-11,但以上小分子的成药性不足。因此,为了进一步提高其活性、选择性及成药性,研究团队继续通过基于结构的药物设计方法开发了具有良好成药性的小分子抑制剂CHMFL-BTK-85。蛋白及细胞层次上的研究表明,CHMFL-BTK-85能够在BTK与EGFR、ITK、JAK3、HER2等激酶间取得选择性。与已上市的BTK抑制剂依鲁替尼相比,其能够显著降低对免疫细胞介导的ADCC的抑制作用。在连续给药14天的小鼠毒理实验中,CHMFL-BTK-85在800mg/kg/day的剂量下未发现明显毒性。这些实验结果进一步验证了选择性的BTK抑制剂在临床应用上可能具有更高的安全性。在动物体内药效评价方面,CHMFL-BTK-85在100mg/kg/day的剂量下能够显著地抑制TMD8细胞构建的小鼠皮下移植瘤的生长,抑瘤率(TGI)达到96%,其在REC-1细胞构建的小鼠原位瘤模型上能够显著延长动物的生存时间。
目前研究团队正在对CHMFL-BTK-85进一步开展临床前成药性评价,以期迅速推动该药物进入产业化开发阶段。该研究获得了“重大新药创制”国家科技重大专项、国家自然科学基金、博士后基金特别资助、中科院前沿科学重点研究计划等项目的支持。
文章链接:https://www.nature.com/articles/s41392-020-00309-1。
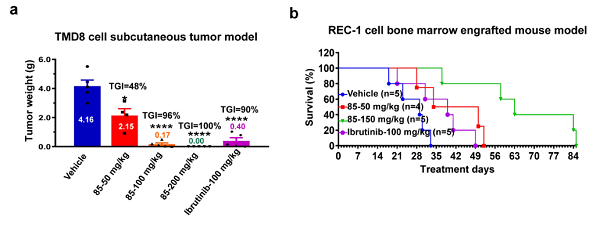
CHMFL-BTK-85的体内抗肿瘤药效学研究